Att efterlikna fysiologiska förhållanden hjälper forskare att hitta metallbindemedel
Forskare har utvecklat en metod för att identifiera små molekyler som binder metalljoner.Metalljoner är viktiga i biologin.Men att identifiera vilka molekyler - och särskilt vilka små molekyler - dessa metalljoner interagerar med kan vara utmanande.
För att separera metaboliter för analys använder konventionella metabolomiska metoder organiska lösningsmedel och låga pH-värden, vilket kan få metallkomplex att dissociera.Pieter C. Dorrestein från University of California San Diego och medarbetare ville hålla samman komplexen för analys genom att efterlikna de naturliga förhållandena som finns i celler.Men om de använt fysiologiska förhållanden under separationen av molekyler, skulle de ha behövt optimera separationsförhållandena för varje fysiologiskt tillstånd de ville testa.
Istället utvecklade forskarna en tvåstegsmetod som introducerar fysiologiska förhållanden mellan en konventionell kromatografisk separation och en masspektrometrisk analys (Nat. Chem. 2021, DOI: 10.1038/s41557-021-00803-1).Först separerade de ett biologiskt extrakt med hjälp av konventionell högpresterande vätskekromatografi.Sedan justerade de pH för flödet som lämnade den kromatografiska kolonnen för att efterlikna fysiologiska förhållanden, tillsatte metalljoner och analyserade blandningen med masspektrometri.De körde analysen två gånger för att få masspektra av små molekyler med och utan metaller.För att identifiera vilka molekyler som binder metaller använde de en beräkningsmetod som använder toppformer för att sluta sig till samband mellan spektra av bundna och obundna versioner.
Ett sätt att ytterligare efterlikna fysiologiska tillstånd, säger Dorrestein, skulle vara att lägga till höga koncentrationer av joner som natrium eller kalium och låga koncentrationer av metallen av intresse.”Det blir ett tävlingsexperiment.Det kommer i princip att säga dig, OK, den här molekylen under dessa förhållanden har mer benägenhet att binda natrium och kalium eller den här unika metallen som du har lagt till, säger Dorrestein."Vi kan infundera många olika metaller samtidigt, och vi kan verkligen förstå preferensen och selektiviteten i det sammanhanget."
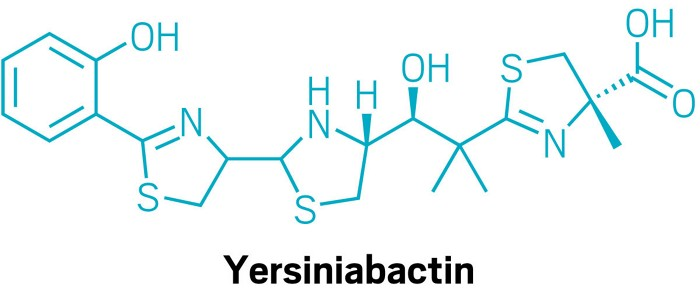
I kulturextrakt från Escherichia coli identifierade forskarna kända järnbindande föreningar som yersiniabactin och aerobactin.När det gäller yersiniabactin upptäckte de att det även kan binda zink.
Forskarna identifierade metallbindande föreningar i prover lika komplexa som löst organiskt material från havet."Det är absolut en av de mest komplexa proverna jag någonsin har tittat på," säger Dorrestein."Det är förmodligen lika komplext som, om inte mer komplext än, råolja."Metoden identifierade domoinsyra som en kopparbindande molekyl och föreslog att den binder Cu2+ som en dimer.
"En omics-metod för att identifiera alla metallbindande metaboliter i ett prov är extremt användbar på grund av vikten av biologisk metallkelering", skriver Oliver Baars, som studerar metallbindande metaboliter producerade av växter och mikrober vid North Carolina State University, i en e-post.
"Dorrestein och medarbetare tillhandahåller en elegant, välbehövlig analys för att bättre undersöka vad metalljonernas fysiologiska roll i cellen kan vara", skriver Albert JR Heck, en pionjär inom infödd masspektrometri vid Utrecht University, i ett mejl."Ett möjligt nästa steg skulle vara att extrahera metaboliterna under naturliga förhållanden från cellen och fraktionera dessa även under naturliga förhållanden, för att se vilka metaboliter som bär vilka endogena cellulära metalljoner."
Kemi & ingenjörsnyheter
ISSN 0009-2347
Copyright © 2021 American Chemical Society
Posttid: 2021-12-23

